肝细胞癌
作者: 医知苑
最后更新时间: 2024-04-08
作者: 医知苑
最后更新时间: 2024-04-08
介绍
90%的病例中,肝脏恶性肿瘤是其他原发性癌症的转移,原发性肝脏恶性肿瘤相对罕见。在原发性肝癌中,90%是肝细胞癌(HCC),其余为肝内胆管癌。
肝细胞癌是全球第六大常见癌症,也是癌症死亡的第二大原因。全球范围内的发病率差异很大,主要取决于乙型肝炎 病毒(HBV)和丙型肝炎 病毒(HCV)感染的发病率;在中国,每10万人中有超过400例病例,而在英国,每10万人中只有约13例病例。
在英国,大多数病例发生在70 岁以上的人群中,其中约 65% 的病例发生在男性;在乙肝或丙肝感染率高的地区,诊断年龄要低得多。
病因学
HCC 通常是由影响肝脏的慢性炎症过程引起的,80-90% 的病例是在已患有肝硬化的情况下出现的。
炎症的病因主要是病毒性肝炎,但导致 HCC 的其他原因包括慢性酒精过量、遗传性血色素沉着病、原发性胆汁性肝硬化 (PBC) 和黄曲霉毒素暴露(一种有毒真菌代谢物)
风险因素
发生 HCC 的主要危险因素是:
-
肝硬化
- 病毒性肝炎感染,主要是乙型肝炎病毒和丙型肝炎病毒、酗酒、非酒精性脂肪肝以及其他罕见原因,包括代谢(遗传性血色病、威尔逊氏病)和自身免疫(原发性胆汁性肝硬化)过程
-
黄曲霉毒素暴露
- 特别是合并乙肝病毒感染时
- 肝细胞腺瘤*
- 抽烟
- 高龄(>70岁)
- 阳性家族史
*病变 > 4cm 的女性约有 5% 发生恶变的风险,任何大小病变的男性发生恶变的风险约为 50%
临床表现
发达国家的许多病例是通过影像学监测发现的,这些患者被确定为高危患者(例如已知的肝硬化患者)。
不太常见的是,患者可能会出现非特异性全身症状,例如疲劳或体重减轻。 HCC 中的腹痛*并不常见,尤其是在疾病的早期阶段。
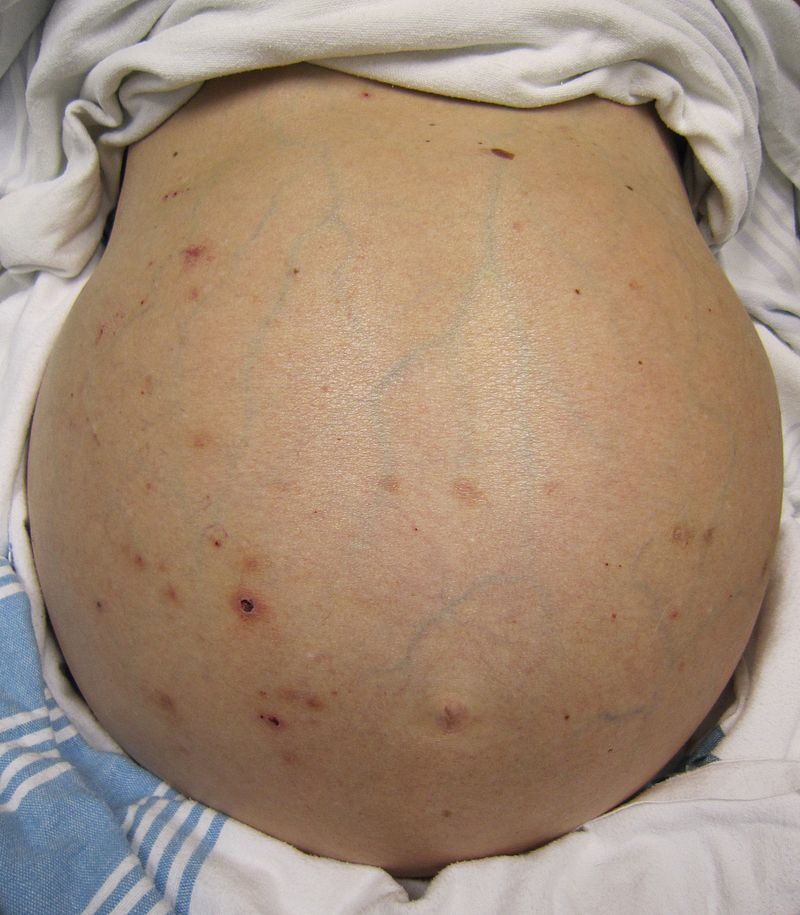
检查时,通常可触及不规则肿大的肝脏,但在早期 HCC 疾病中,可能不会出现这种情况。那些已经患有肝病的人可能会出现失代偿性肝病的特征,例如腹水、黄疸或精神错乱。
*少数患者会出现肿瘤破裂,伴有出血继发的疼痛,或更罕见的情况是血流动力学受损
调查
实验室测试
疑似 HCC 患者应进行血常规检查,包括全血细胞计数、肝功能检查和凝血情况。
应在所有疑似病例中测量甲胎蛋白(AFP) 水平,但在确诊病例中,甲胎蛋白(AFP) 水平通常不会升高,并且最适合用于衡量既往诊断患者的疾病反应或监测。
影像学
超声扫描是高危人群筛查 HCC 的首选成像方式。 HCC 病变在超声上显示为低密度异质性病变,但通常很难与任何背景肝硬化(如果存在)区分开来。
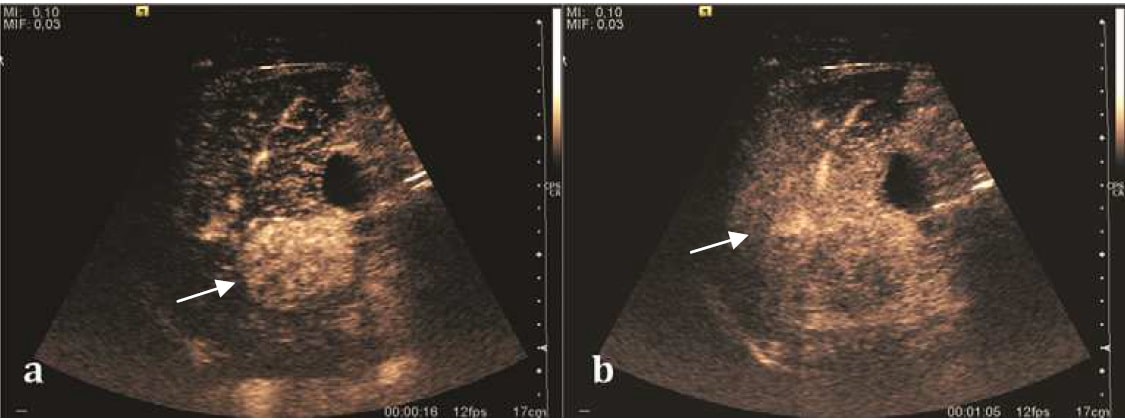
超声造影(图 3)已用于研究肝脏病变的动脉化,以帮助诊断可疑病变中的 HCC。
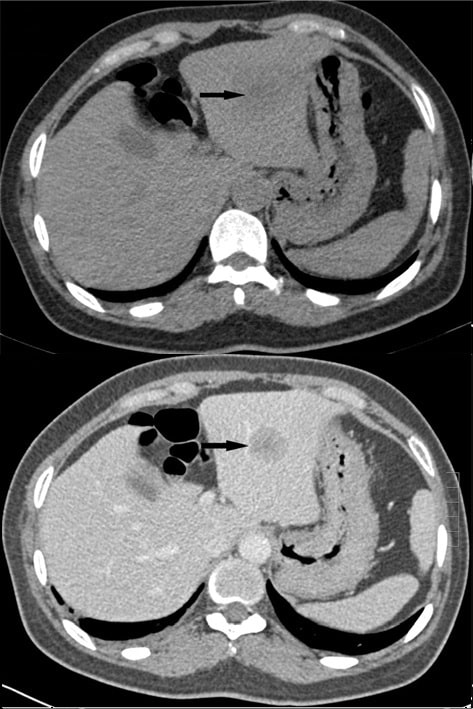
MRI 成像或CT 成像(图 4)都可用于进一步评估超声识别的病变。这些成像方式通常显示在动脉晚期阶段生动增强的肿块以及随后的快速消退。
如果病例特征明确且具有典型的 HCC 影像学特征,则可以通过放射学诊断。如果不满足这些要求,则可以通过超声引导或 CT 引导的经皮活检进行活检以进行组织学诊断。由于肿瘤沿针道种植的风险 (1-5%),这应该在有经验的中心进行。
分期
巴塞罗那临床肝癌分期系统(BCLC) 是最受接受和广泛使用的HCC 分期。它根据肿瘤大小和肿瘤数量以及肝功能*、身体状况和癌症相关症状来确定肿瘤分期。这些因素用于将阶段定义为 0(极早期)、A(早期)、B(中期)、C(高级)和 D(末期),并进一步表征,以便定义治疗计划和预后。
*肝功能主要由 Childs-Pugh 评分来定义,该评分根据血清胆红素和白蛋白水平、INR 以及是否存在腹水和肝性脑病及其程度进行评分
管理
肝细胞癌的治疗应由多学科团队讨论决定,包括肝病学、肝胰胆外科、诊断和介入放射学以及肿瘤内科。
治疗方案可分为局部治疗或全身治疗、治愈性治疗或姑息性治疗。治疗选择包括肝移植或肝切除形式的手术,以及使用微波或射频消融的消融技术。肝移植消除了肝硬化患者 HCC 的根本病因,因此复发的风险非常低,而肝切除和消融治疗不能解决肝硬化,复发通常出现在残余实质中。
对于患有转移性疾病的患者,需要进行全身治疗,即抗血管生成药物,如索拉非尼和阿替利珠单抗。这些疗法也用于患有不适合移植、切除、消融或栓塞的弥漫性肝内疾病的患者。
手术管理
对于没有肝硬化或肝硬化非常轻微且不符合肝移植标准的患者,手术切除和淋巴结清扫是首选治疗方法。这可以是解剖性或非解剖性(楔形)切除,具体取决于肿瘤的大小和位置。大约 15% 的 HCC 被认为适合手术切除,主要是那些具有单灶性病变的HCC 。
切除后,残余肝脏必须至少占肝脏总体积的20-40%,以减轻肝切除术后肝衰竭的风险。通过术前对供应待切除肝脏一侧的门静脉进行门静脉栓塞,可以使残余体积最大化。切除后,肝脏能够再生到所需的大小。
肝移植仅用于符合米兰标准的病例:
- 1 个病灶 < 5 厘米或最多 3 个病灶均 < 3 厘米
- 没有血管浸润
- 无肝外表现
根据这些标准,肝移植的5 年生存率为 60-75%。肝移植术后死亡率高达 10% 左右,并且还需要终生免疫抑制。由于供体器官短缺,大多数患者还将在移植等待名单上等待很长时间,因此可能需要临时治疗以防止病情进展,例如切除、消融或化疗栓塞。
非手术治疗
消融
消融可以在图像引导下经皮进行,或者在手术中进行,通常是在切除其他病变时,作为混合手术的一部分。消融适用于肿瘤大小不超过 3 厘米、不超过 3 个肿瘤、无肝硬化或轻度肝硬化的肿瘤,并且肿瘤必须在超声或 CT 上可见,以便放置探头。
消融最适合用于需要进行主要肝切除术的深部小肿瘤以及不适合手术的患者。消融最常通过射频(RFA) 或微波(MWA) 进行;已经进行了冷冻消融和注射酒精,但效果较差。
早期 HCC 的切除和消融的结果没有显着差异。因此,消融可用作主要治疗方法,也可用作等待肝移植患者的新辅助治疗。
经动脉化疗栓塞术
HCC 几乎所有的血液供应都来自肝动脉系统(与正常肝实质的门静脉不同)。经动脉化疗栓塞(TACE)通过选择性栓塞肿瘤的动脉来利用这一点,导致肿瘤缺血和坏死。
栓塞是通过在放射学引导下将化疗和栓塞剂注射到供应肿瘤的超选择动脉中来实现的。 TACE 保留用于 BCLC B 期患者,肿瘤结节边界清楚,不适合切除或移植。虽然 TACE 不能治愈,但已被证明可以提高生存率并且发病率较低。
预后
肝细胞癌的预后取决于潜在肝硬化的程度,因为这在决定癌症治疗的积极程度以及患者的肝脏疾病负担方面发挥着重要作用。
假设没有或轻度肝硬化,每种治疗途径的预期 5 年生存率为:
- 肝移植 60-75%
- 肝脏切除 45-70%
- 消融 68%(肿瘤 <2cm)
- 动脉化疗栓塞 26%
继发性肝转移
由于通过门脉循环扩散,大约一半的肝脏转移来自结直肠原发肿瘤。然而,任何实体器官肿瘤都可以转移到肝脏,其次是胰腺、乳腺癌和肺。
这些通常是在初步诊断后通过分期成像发现的。然而,患者可能会出现黄疸或右上腹疼痛。
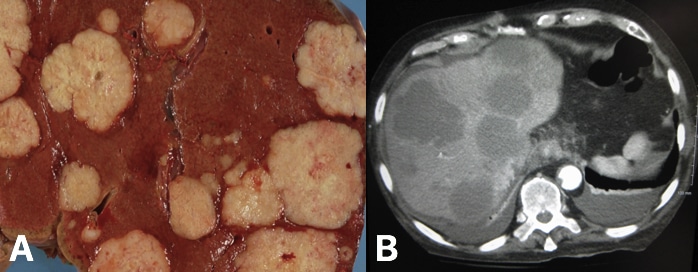
图 6 – 转移性肝脏 (A) 来自原发结肠的转移性肝脏沉积物,尸检 (B) CT 扫描显示转移性肝脏沉积物
从历史上看,任何原发性肝转移的患者都被认为是无法治愈的,姑息治疗是主要的治疗方法。然而,现在结直肠转移(以及黑色素瘤、神经内分泌肿瘤(NET)、睾丸癌或卵巢癌的转移)可以考虑进行手术治疗以提高生存率。
肝转移瘤的治疗方案与原发性肝肿瘤的治疗方案大致相似,可以进行手术切除、消融和TACE 。在少数选定的病例中,主要是 NET,可以考虑肝移植。
考虑以治愈为目的的切除,从而可以保留足够大的功能性肝脏残余物,同时实现疾病的肿瘤清除。
关键点
- 肝细胞癌(HCC)最常与继发于肝炎病毒感染或过量饮酒的肝硬化相关
- AFP 水平对于监测治疗反应和复发最有用
- 巴塞罗那临床肝癌分期系统可以确定治疗和预后
- 手术和非手术选择都可以治愈,包括肝切除或移植和消融
- 转移至肝脏的最常见癌症是肠癌、胰腺癌、乳腺癌和肺癌