肝脏移植
作者: 医知苑
最后更新时间: 2024-04-15
作者: 医知苑
最后更新时间: 2024-04-15
介绍
肝移植(LT)适用于治疗急性肝衰竭(ALF)和终末期肝病(ESLD)。目前,LT 后患者的总体 1 年和 5 年生存率分别为 80-90% 和 60-75%。
肝移植根据供体类型可分为死体肝移植和活体肝移植。
西方国家约 95% 的肝移植主要来自已故捐赠者*。原位肝移植(OLT)是迄今为止最常见的手术,其中切除自体肝脏,然后用相同解剖位置的供体肝脏替换。
虽然大多数肝移植是整个器官的移植,但也可以进行分段肝移植或减量移植。
- 分段(或分割)肝移植允许移植两个受者(通常是成人和儿童)同一个尸体器官
- 减少移植物可适应供体和受体体型不匹配的情况
*活体肝脏捐赠,即仅从活体捐赠者处移植部分肝脏,是远东(例如日本和韩国)以及其他一些对死后埋葬有文化信仰和习俗限制的国家器官捐赠的主要来源已故捐献者的整个器官移植
适应症
在西方国家,肝移植最常见的适应症是慢性 HCV 感染导致的终末期肝病(ESLD) 、酒精性肝病(ALD) 或非酒精性脂肪肝病(NAFLD)。
其他条件包括:
-
非胆汁淤积性肝病
- 慢性 HBV 感染、自身免疫性肝炎或隐源性肝炎
-
胆汁淤积性肝病
- 原发性胆汁性肝硬化 (PBC) 或原发性硬化性胆管炎 (PSC)
-
代谢性肝脏疾病
- Alpha-1-抗胰蛋白酶缺乏症、威尔逊病、遗传性血色素沉着症或克里格勒-纳贾尔综合征
-
原发性肝脏恶性肿瘤
- 肝细胞癌、肝母细胞瘤或肝门部胆管癌
- 布加综合征
- 药物引起的急性肝衰竭
终末期肝病的严重程度可以通过终末期肝病模型(MELD) 评分系统进行评估,该系统根据患者的 INR、胆红素、肌酐和钠进行计算,估计患者的生存率,并用于对患者进行优先治疗移植等待名单。
急性肝衰竭被定义为在没有预先存在的肝病的情况下发生严重脑病和凝血病,可以根据国王学院标准进行分类,这也有助于确定最能从 LT 中受益的患者。
禁忌症
肝移植禁忌症可分为绝对禁忌症和相对禁忌症。
|
绝对 |
相对的 |
|
不受控制的败血症
酗酒或滥用药物,或持续不坚持药物治疗 晚期心脏或肺部疾病 肝外恶性肿瘤 |
多系统器官衰竭伴暴发性肝衰竭
活动性感染 高龄、虚弱或广泛的合并症 耐药性乙型肝炎肝硬化 |
表 1 – 肝移植的禁忌症
手术技术
LT 的两个关键步骤是器官取出和受体植入。供体-受体匹配主要基于ABO血型相容性和移植物与受体重量比(GRWR)。基于 HLA 的兼容性对于 LT 来说并不是必需的。
捐赠程序
根据死者捐献的类型,器官检索途径也有所不同。这可以分为脑干死亡后捐赠 (DBD)或循环死亡后捐赠(DCD)。
DBD检索
对于DBD 供体的肝脏检索,通过中线剖腹手术和开胸手术获得腹部和胸部的完全暴露。肝脏被动员起来,胆总管被解剖,胆囊被排空并冲洗。在交叉夹闭胸降主动脉之前,对供体进行肝素化并全身灌注冷藏液。
肝脏被迅速从体内移除,留下与主动脉补片上的腹腔轴连续的肝总动脉。切开肝下和肝上 IVC,以便取出肝脏,整个IVC 位于其下方。在运输之前,将器官从体内取出,放在后桌上的冰上,以进行进一步的门静脉灌注。
DCD检索
对于DCD 供体的肝脏检索,一旦确认心脏停搏,就会进行快速剖腹手术和开胸手术。主动脉被交叉夹紧,冷灌注液通过插管主动脉注入,以尽量减少热缺血时间。通过门静脉插管建立门静脉灌注。该程序的其余部分与 DBD 供体中的冷相解剖是模棱两可的。
接收程序
接收程序由两个步骤组成;肝切除术和肝移植植入术。
肝切除术有两种类型:经典方法(图 3)切除受者 IVC 或背负式技术 (图 4)保留 IVC。经典方法的特点是静脉回流中断并伴有显着的血流动力学变化,因此在可行的情况下通常选择背驮式技术。
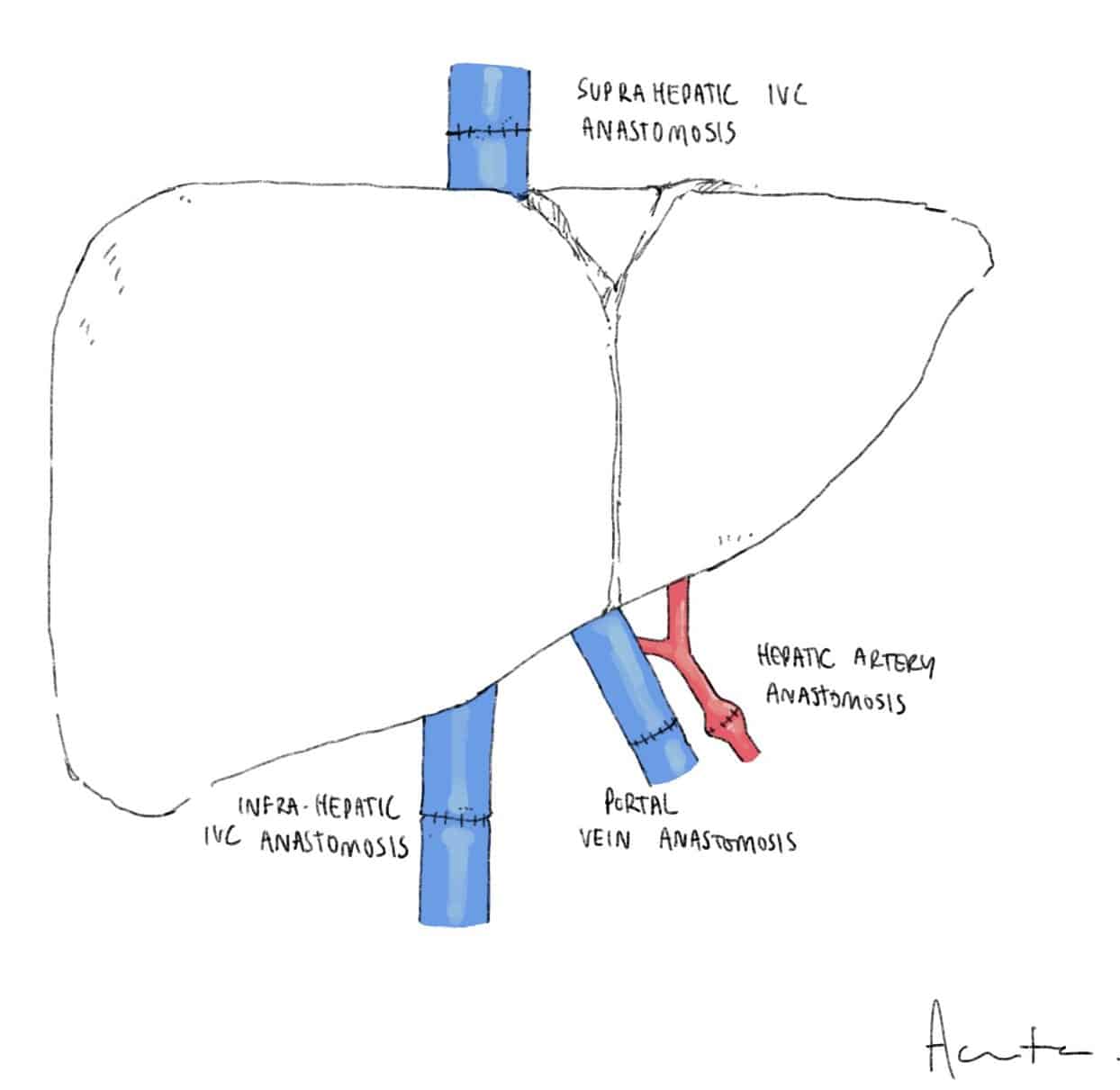
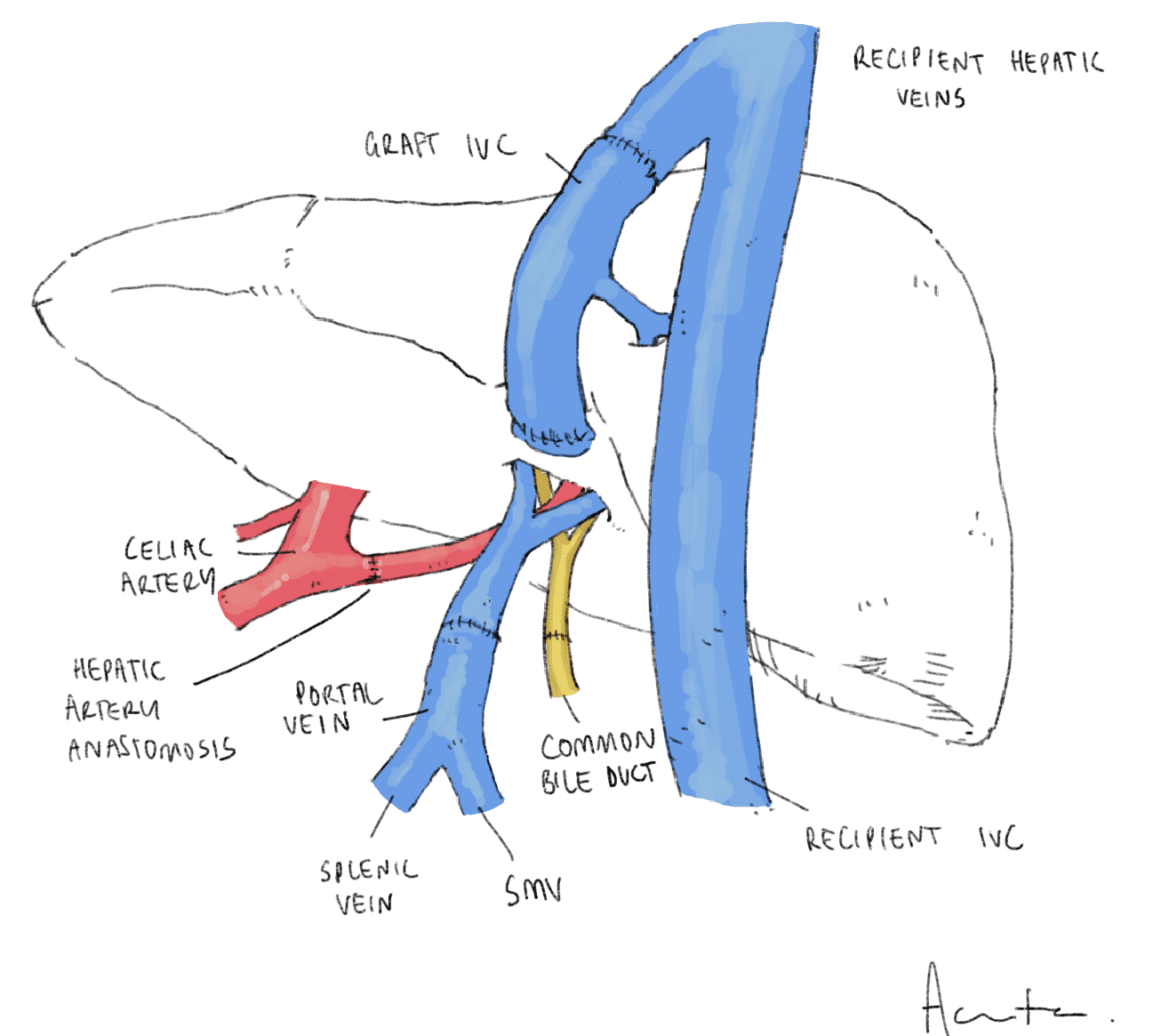
根据选择的肝切除术类型,植入将是静脉替代移植或背驮式植入。在背驮式植入的情况下,供体 IVC 可以并排连接到受体 IVC 或肝上端吻合到受体肝静脉。
在这两种情况下,供体和受体的门静脉和肝动脉都是端对端吻合的。胆管吻合术的首选类型是管对管或 Roux-en-Y 肝空肠吻合术(例如在 PSC 患者中,因为受者胆管患病)。
肝移植的并发症
LT 后的并发症很常见,第一年内的死亡率为 5-10%。术后出血是最常见的手术并发症(15%)。
移植物原发性无功能
移植物功能障碍最严重的形式是原发性无功能,这是一种极端形式的保存损伤,可阻止血运重建后移植物的恢复。其发生率在1-3%之间。
其临床表现为急性肝功能衰竭,伴有黄疸、凝血病、脑病和血清转氨酶水平升高,但无血管并发症。
DCD移植物冷缺血时间延长、热缺血时间延长以及脂肪肝是主要危险因素。再次移植是目前唯一的治疗选择。
血管并发症
LT 后最常见的血管并发症是肝动脉血栓形成(HAT)、门静脉血栓形成(PVT) 和静脉流出道阻塞:
-
HAT是 LT 后最常见的血管并发症,通常发生在供体肝动脉和受体肝动脉之间的吻合部位,表现为移植失败
- 多普勒超声可检测HAT, CT动脉造影可确诊;治疗选择范围从介入血管内技术到手术翻修或再次移植
-
PVT表现为移植失败(如果是早期 PVT)或门脉高压症状(如果是晚期 PVT)
- 还可以使用多普勒超声和CT 门静脉造影进行诊断(图 5);早期病例需要进行手术翻修和重新移植,但晚期病例通常可以保守治疗
- 下腔静脉 流出道阻塞的情况很少见,可通过颈静脉造影和压力梯度测量来帮助诊断;支架置入术或球囊血管成形术的血管内介入治疗通常是首选治疗方法
胆道并发症
胆道并发症包括渗漏或狭窄,发生在 10-20% 的 LT 中,大多数发生在移植后的前三个月内。
胆漏几乎总是在术后早期出现,患者可能出现局部腹膜炎或败血症的体征。
胆道狭窄可分为吻合性或非吻合性(缺血性胆管病):
- 吻合口胆管狭窄出现在术后晚期,并伴有进行性胆汁淤积; MRCP 可以明确诊断,ERCP 加支架置入或扩张通常是治疗选择
- 缺血性胆管病涉及胆管树节段性狭窄,主要危险因素是冷缺血时间过长;治疗可能很困难,如果广泛存在,可能需要重新移植
拒绝
大约 25-50% 的肝移植受者在移植后第一年会发生急性排斥反应。他们通常在随访期间被诊断为肝功能检查异常,需要通过肝活检来确诊。
治疗取决于急性排斥反应的严重程度,范围从免疫抑制剂量调整到高剂量静脉注射 皮质类固醇或多克隆抗体。
长期并发症
LT 的其他并发症包括全身性高血压(以及缺血性心脏病)、新发糖尿病(通常继发于糖皮质激素或长期使用钙调磷酸酶抑制剂)、肾功能损害(也由于使用钙调磷酸酶抑制剂导致血糖控制不佳)、糖尿病传播未检测到的供体疾病(感染或恶性肿瘤)、原发性肝病复发和慢性排斥反应。
关键点
- 肝移植适用于治疗急性肝衰竭和终末期肝病
- 大多数肝移植是通过原位肝移植(OLT)进行的,即切除自体肝脏,然后用相同解剖位置的供体肝脏替换
- 排斥反应、胆道并发症和血管并发症(包括出血)是术后并发症的主要来源
- 肝移植后五年生存率为 60-75%